팬젠은 위탁기관으로부터 올 1월 말 EPO 바이오시밀러(바이오의약품 복제약) 'PDA10'의 임상3상 결과를 받았다. 2014년 2월 환자 모집을 시작한 이후 3년여 만이다.
팬젠은 3상 결과 PDA10이 오리지널약인 암젠의 '이플렉스'와 동등성을 입증했다고 설명했다. 유럽의약국(EMA)과 한국 식품의약품안전처의 바이오시밀러 평가 기준을 모두 충족했다는 것이다. 이에 따라 말레이시아와 한국에서의 판매 허가 획득을 기대하고 있다.
◆ 말기 신부전 환자 298명 대상 3상 진행
EPO(erythropoietin)는 적혈구 생성에 관여하는 물질로 빈혈치료제로 쓰인다. 적혈구의 부족은 빈혈을 불러오는 요인 중 하나다. EPO는 신장에서 만들어진다.
팬젠은 PDA10 3상을 혈액 투석이 필요한 말기 신부전 환자들을 대상으로 했다. 이들은 빈혈 증상을 동반하고 있는데, 신장의 기능이 떨어지면서 정상적인 EPO 생산에 문제가 생겼기 때문이다.
말기 신부전 환자들을 피험자로 쓴 또다른 이유 중의 하나는, PDA10이 1세대 EPO의 바이오시밀러기 때문이다. 1세대 EPO는 통상적으로 일주일에 3회 정도 투약한다. 말기 신부전 환자 역시 일주일에 약 3회의 혈액 투석이 필요하다. 혈액 투석을 위해 병원을 찾을 때 EPO를 투약받는 것이 일반적이다.
이종민 개발담당 이사는 "이러한 특성 때문에 선진국에서도 1세대 EPO가 시장의 60%를 차지하고 있다"며 "1세대 EPO는 꾸준히 시장의 일정 부분을 차지할 것"이라고 말했다.
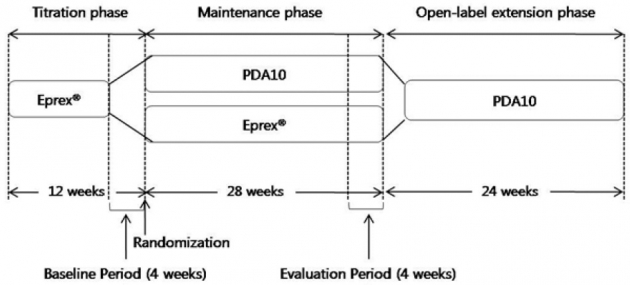
PDA10의 3상은 한국과 말레이시아에서 이뤄졌다. 한국 70명과 말레이시아 228명을 무작위 배정했고, 의사와 환자가 모두 대조약과 시험약 여부를 모르는 이중 눈가림 방식이었다.
우선 12주간 이플렉스를 투여해 피험자들의 상태를 유사하게 만든다. 이후 28주간 각각 PDA10과 이플렉스 투여군으로 나눠 두 그룹의 동등성을 평가한다. 마지막 과정에서는 PDA10만 24주를 투여해 장기 안전성과 내약성을 평가했다.
이는 EMA와 한국 식약처의 바이오시밀러 임상 가이드라인을 따른 것이다. 또 이플렉스의 첫번째 바이오시밀러인 산도즈의 '비노크리트' 3상과 동일하다.
◆ 비노크리트 대비 우수한 동등성 확인
팬젠 측은 PDA10의 임상3상에서 비노크리트보다 우수한 동등성을 확인해 고무돼 있다.
빈혈치료제의 효능은 적혈구 속에서 산소를 운반하는 헤모글로빈의 수치로 측정한다. 정상인의 경우 혈액 1dl당 13~15g의 헤모글로빈이 있다. 빈혈 환자는 8~9g, EPO의 목표치는 이를 10~12g 수준까지 올리는 것이다.
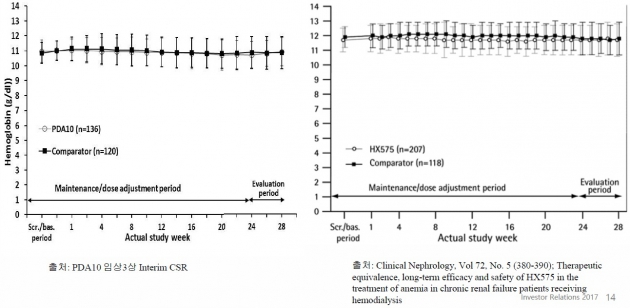
팬젠은 3상에서 이플렉스 투여군과 PDA10 투여군의 헤모글로빈 수치를 비교했다. 28주간의 관찰 결과 PDA10과 이플렉스 투여군의 헤모글로빈 수치는 거의 동일한 궤적을 그렸다. 비노크리트와 이플렉스 비교 결과보다 더 흡사한 모습이다.
EMA와 식약처의 EPO 바이오시밀러 동등성 판정 기준은 이렇다. 오리지널약의 헤모글로빈 수치 변화량 평균과 바이오시밀러의 평균간의 차이가 dl당 ±0.5g 사이에 있어야 한다. PDA10과 비노크리트는 모두 이 조건을 충족하고 있다. 특히 PDA10은 비노크리트 대비 변화량 차이가 더 작아 이플렉스와 더 유사한 것으로 나타났다.
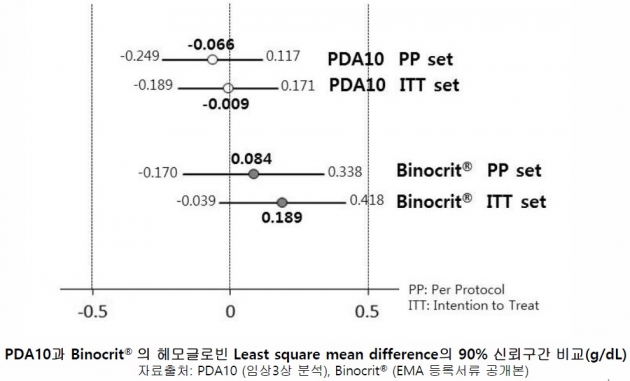
PDA10의 이플렉스 투여군과의 변화량 차이는 -0.066(PP set 기준)이었다. 비노크리트는 3상에서 0.084를 기록했었다. 이 수치는 0이면 똑같다는 것이고, 0과 근접할수록 유사하다는 의미다. 'PP set'은 임상 계획대로 최종까지 투여가 이뤄진 피험자, 'ITT set' 임상 탈락자를 포함한 모든 피험자들의 수치를 말한다.
팬젠은 임상3상의 자세한 결과를 학술지를 통해 발표할 계획이다. 또 3상의 결과를 바탕으로 이달 말레이시아, 2분기 한국 신약허가(NDA)를 신청할 예정이다.
특히 말레이시아 환자를 대상으로 임상시험한 최초의 EPO 바이오시밀러라는 점, 말레이시아가 오리지널약과 바이오시밀러의 판매만 허용한다는 점에서 말레이시아에서의 선전을 기대하고 있다.
한민수 한경닷컴 기자 hms@hankyung.com
기업의 환율관리 필수 아이템! 실시간 환율/금융서비스 한경Money
관련뉴스













