앱클론은 미국 임상종양학회(ASCO)에서 키메릭 항원 수용체 T세포(CAR-T) 치료제 'AT101'의 혈액암 임상1상 후속 데이터를 발표했다고 4일 밝혔다.
이 데이터는 임상1상 투여 후 약 2년간 환자들의 치료 효과를 확인한 연구 결과다. 추적기간 중간값 16.4개월의 평가 결과에서 AT101은 기존 CAR-T 치료제 대비 우월한 치료 효과를 입증했다. 임상1상 평가에서 완전관해를 보였던 피험자 9명 중 7명이 12개월 이상 완전관해를 유지했으며, 장기간 완전관해 비율은 77.8%에 달했다.
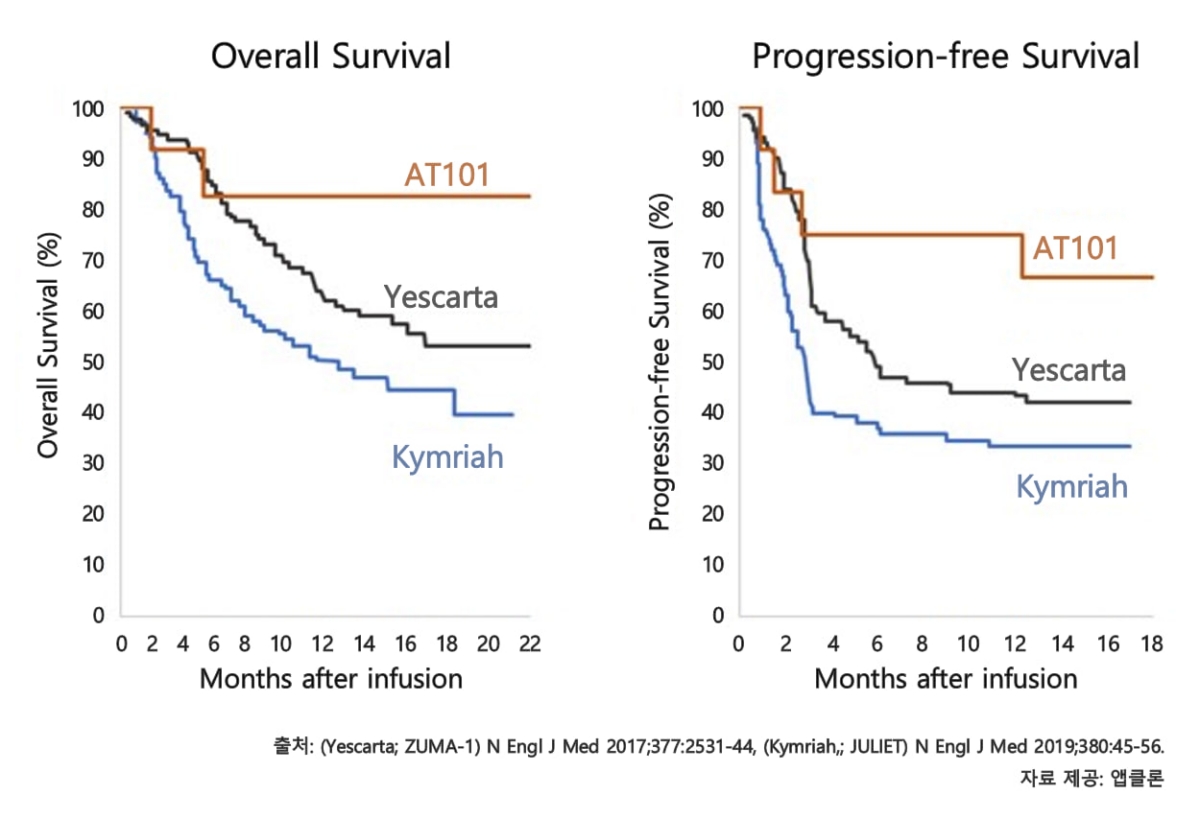
AT101 임상1상의 낮은 투여농도 구간의 피험자는 6명이며, 전체 결과의 절반을 차지한다. 임상2상의 4%에 해당하는 매우 적은 양을 투여한 환자를 포함했음에도 불구하고 전체생존율(OS) 82.5%, 무진행생존율(PFS) 66.7%의 결과를 보였다.
현재 판매되고 있는 예스카타와 킴리아의 임상2상 결과 발표 논문에 따르면 12개월 시점의 전체생존율은 각각 59%, 49%를 기록했다. 특히 예스카타의 15개월 무진행생존율은 41%로 알려져 있다. AT101의 임상1상을 글로벌 임상2상 결과와 직접적으로 비교하는 것은 무리가 있으나 기존 카티 치료제 대비 압도적으로 우수한 결과라고 회사측은 설명했다.
AT101의 연속된 암세포 살상능력 및 장시간 약효 유지로 인한 강력한 항암 활성 특성은 해외 학술지 및 학회에서 여러 차례 보고된 바 있다. 해당 연구는 미국 펜실베니아 의과대학, 서울대학교 의과대학 등과 공동연구로 이뤄졌다.
앱클론의 CAR-T 치료제 기술 적용 결과 앱클론의 인간화 항체 'h1218'를 이용한 AT101은 기존 CAR-T 치료제보다 높은 75%의 완전관해율(CR)과 91.7%의 객관적 반응률(ORR)을 보였다. 특히 임상1상의 중간용량 및 고용량 투여군 6명에 대해서는 100% 완전관해를 보였다.
앱클론 관계자는 "임상1상에서 확보한 AT101의 유효성과 안전성을 기반으로 현재 임상2상을 진행중"이라며 "AT101 치료 효과의 지속성으로 혈액암 환자 질환의 완전한 치료와 극복이 가능하다고 판단한다"고 말했다.
그는 이어 "기존 카티 치료제에 불응하는 환자에 대한 치료 효과도 확보하고자 노력중"이라며 "AT101이 새로운 글로벌 혈액암 치료제 시장을 열 가능성을 높이고 있다"고 덧붙였다.
관련뉴스













